Je tombe sur un article d’une équipe belge, article dont le thème m’accroche. (Xie et al. 2023)
Je passe le début de l’article par Google traduction. À suivre …
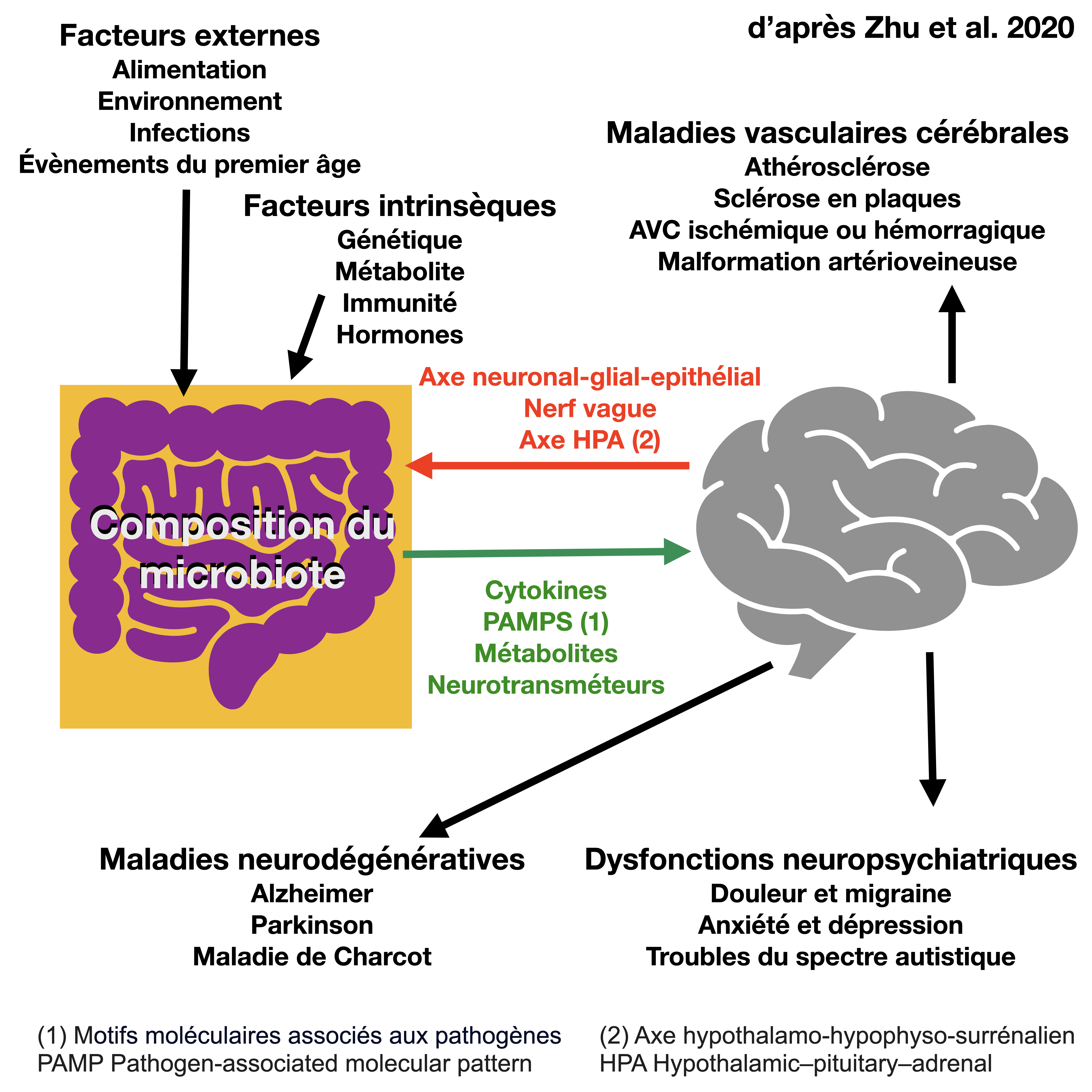
Le microbiote intestinal est constitué de micro-organismes, notamment de bactéries, d’archées, de virus, de champignons et de protozoaires, qui vivent dans le tube digestif en symbiose avec l’hôte. Au cours de la dernière décennie, le microbiote intestinal a fait l’objet de nombreuses études et a démontré son importance pour de nombreuses fonctions biologiques de l’organisme, notamment le développement intestinal, l’intégrité et la fonction de la barrière intestinale (Hooper, 2004 ; Backhed et al., 2005), le métabolisme (Visconti et al., 2019 ; Agus et al., 2021) et la régulation des réponses immunitaires périphériques et centrales (Hooper et al., 2012 ; Sharon et al., 2016). Bien que le mécanisme de communication entre le microbiote intestinal et le SNC ne soit pas entièrement compris, quatre principales voies de signalisation ont été proposées, notamment les voies immunitaire, endocrine, neurale et humorale (Dalile et al., 2019). Par ces voies, le microbiote intestinal peut affecter (in)directement la physiologie cérébrale, notamment la neurogenèse, la myélinisation, l’activation de la microglie et la régulation des neurotransmetteurs et des facteurs neurotrophiques tels que le facteur neurotrophique dérivé du cerveau et le facteur de croissance nerveuse (Diaz Heijtz et al., 2011 ; Sharon et al., 2016).
Le développement du SNC comprend également la formation d’interfaces hémato-encéphaliques étroitement fermées qui assurent un microenvironnement optimal pour les fonctions du système nerveux central (SNC) en limitant la diffusion paracellulaire et transcellulaire des substances hydrophiles et lipophiles (Strazielle & Ghersi-Egea, 2013). L’une des interfaces hémato-encéphaliques importantes est la barrière hémato-encéphalique (BHE), située au niveau de l’endothélium des microvaisseaux cérébraux, scellé par des jonctions serrées (JT), des astrocytes et des péricytes (Strazielle & Ghersi-Egea, 2013). Français Il existe de plus en plus de preuves que le microbiote intestinal peut affecter l’intégrité de la BHE, les souris traitées aux antibiotiques à large spectre (AB) et les souris sans germes (GF) présentant une perméabilité de la BHE significativement améliorée et une dysrégulation des jonctions interendothéliales des cellules (Braniste et al, 2014 ; Frohlich et al, 2016 ; Hoyles et al, 2018). Le(s) mécanisme(s) par lequel les microbes intestinaux exercent leur influence sur la fonction de la BHE ne sont pas clairs, mais les changements de la physiologie cérébrale induits par l’altération du microbiote intestinal peuvent se produire indépendamment via les voies neuronales vagales ou sympathiques en l’absence de toute réponse immunitaire, indiquant une contribution au moins partielle des métabolites solubles dérivés des microbes (Bercik et al, 2011). Français Les acides gras à chaîne courte (AGCC), les principaux métabolites produits par la fermentation colique des fibres alimentaires et de l’amidon résistant, se sont avérés améliorer l’intégrité de la BHE en régulant positivement l’expression de TJ in vitro et in vivo (Parker et al, 2020). Par exemple, la supplémentation en butyrate a sauvé la perturbation de la BHE chez les souris GF en régulant positivement l’expression de l’occludine (OCLN) et de la claudine-5 (CLDN-5 ; Braniste et al, 2014). Dans un modèle de culture cellulaire, il a été constaté que le propionate atténue la perturbation de la BHE induite par le lipopolysaccharide (LPS) en régulant positivement l’expression de CLDN-5 et de la zone occludens-1 (ZO-1) (Hoyles et al, 2018). Les AGCC peuvent accéder à la BHE par la circulation sanguine et avoir un impact direct sur son intégrité (Macfabe, 2012) ou affecter indirectement sa fonction en activant des récepteurs des acides gras libres (FFAR), tels que FFAR2 et FFAR3, dans les cellules endothéliales (Alexander et al., 2015).
Une autre interface hémato-encéphalique importante, mais souvent négligée, est la barrière hémato-encéphalique (LCR), formée par les cellules épithéliales du plexus choroïde (CPE), étroitement interconnectées par la présence de jonctions choroïdiennes (Strazielle & Ghersi-Egea, 2013). Il existe un nombre croissant de preuves montrant que la barrière hémato-encéphalique joue un rôle crucial dans la propagation des réactions inflammatoires de la périphérie vers le SNC et contribue à la pathogenèse et à la progression de divers troubles neurologiques (Baruch et al, 2015 ; Brkic et al, 2015 ; Gorle et al, 2018 ; Steeland et al, 2018 ; Rodriguez-Lorenzo et al, 2020 ; Van Hoecke et al, 2021 ; Xie et al, 2021).
Références
Définitions
Les métabolites primaires sont directement impliqués dans les processus indispensables au développement normal et à la reproduction de la cellule. Ce sont par exemple des acides aminés, des acides carboxyliques, des alcools, des antioxydants, des nucléotides, des polyols ou encore des vitamines.